ناقلة الأمين (ATA)
الإنزيمات: هي محفزات بيولوجية جزيئية كبيرة، ومعظم الإنزيمات عبارة عن بروتينات.
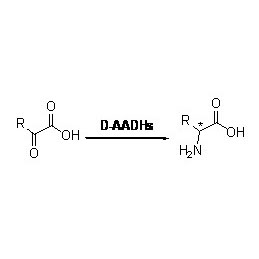
الترانسامينازات: فئة من الإنزيمات التي تحفز نقل الأمين بين الأحماض الأمينية والأحماض الكيتونية. تُعد الترانسامينازات إنزيمات بيولوجية أساسية في التخليق غير المتماثل والفصل الراسيمي للأمينات الكيرالية.
يمكن تقسيم إنزيمات ناقلة الأمين إلى أربع فئات وفقًا للتسلسل والبنية: Ⅰ، Ⅱ، Ⅲ و Ⅳ. تنتمي إنزيمات ناقلة الأمين ω إلى فئة ناقلات الأمين من الفئة الثانية، وتستخدم عادةً في تحضير الأمينات الكيرالية والأحماض الأمينية غير الطبيعية، مثل أحماض بيتا الأمينية.
ω-أمينوترانسفيراز: في معظم الحالات، يشير ω-ترانساميناز إلى فئة من الإنزيمات التي تحفز تفاعلات نقل الأمونيا بدون حمض أميني ألفا كركيزة أو منتج.
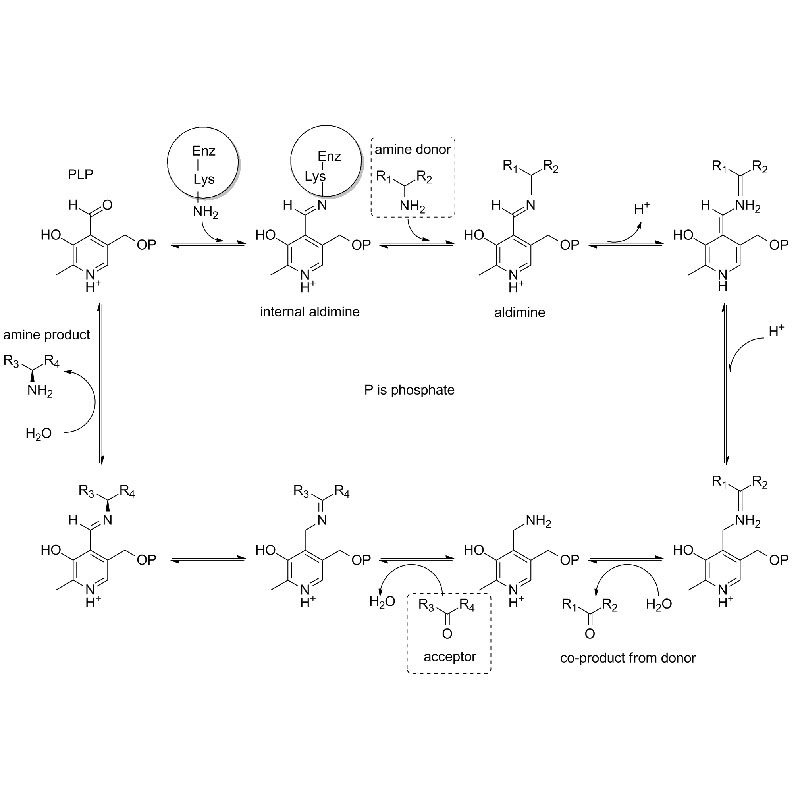
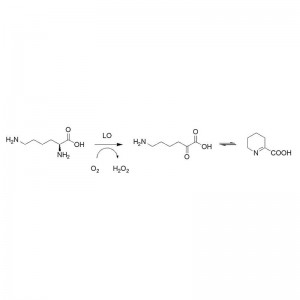
الآلية التحفيزية:
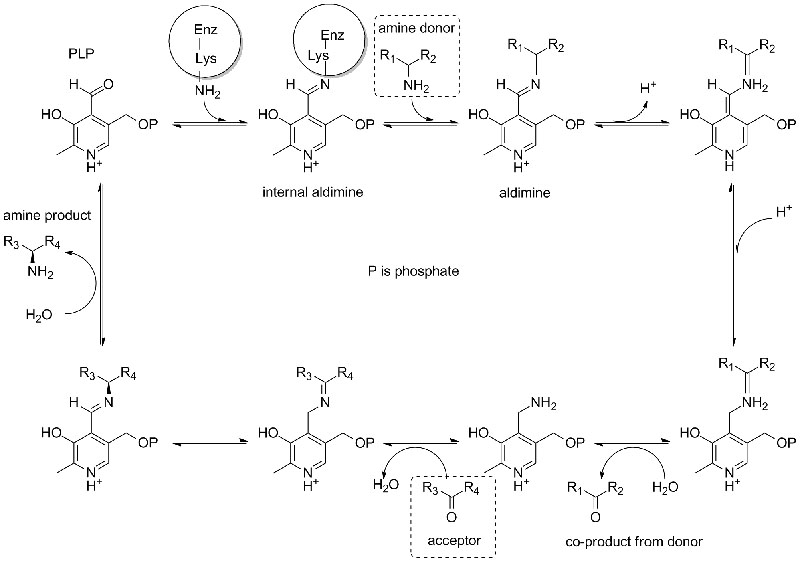
| الإنزيمات | رمز المنتج | رمز المنتج |
| مسحوق الإنزيم | ES-ATA-101~ ES-ATA-165 | مجموعة من 65 إنزيم ناقل أمين أوميغا، 50 ملغ لكل منها، 65 قطعة * 50 ملغ / قطعة، أو كمية أخرى |
| مجموعة الفحص (SynKit) | ES-ATA-6500 | مجموعة من 65 إنزيم ناقل أمين أوميغا، 1 ملغ لكل منها، 65 قطعة * 1 ملغ / قطعة |
★ تخصص عالٍ في الركيزة.
★ انتقائية كيرالية قوية.
★ كفاءة تحويل عالية.
★ منتجات ثانوية أقل.
★ ظروف تفاعل معتدلة.
★ صديق للبيئة.
➢ ينبغي إجراء فحص الإنزيم لركائز محددة بسبب خصوصية الركيزة، والحصول على إنزيم يحفز الركيزة المستهدفة بأفضل تأثير تحفيزي.
➢ تجنب ملامسة الظروف القاسية مثل: درجات الحرارة العالية، ودرجة الحموضة العالية/المنخفضة، والمذيبات العضوية ذات التركيز العالي.
➢ عادةً، يجب أن يتضمن نظام التفاعل الركيزة، والمحلول المنظم، ومانح الأمين (مثل الأحماض الأمينية و1-فينيل إيثيل أمين) أو المستقبل (مثل الأحماض الكيتونية)، والإنزيم المساعد (PLP)، والمذيب المساعد (مثل DMSO).
➢ يجب إضافة ATA أخيرًا إلى نظام التفاعل، بعد ضبط درجة الحموضة ودرجة الحرارة وفقًا لظروف التفاعل.
➢ جميع أنواع ATA لها ظروف تفاعل مثالية مختلفة، لذلك يجب دراسة كل منها على حدة.
مثال 1 (تخليق سيتاغليبتين، التخليق غير المتماثل)(1):
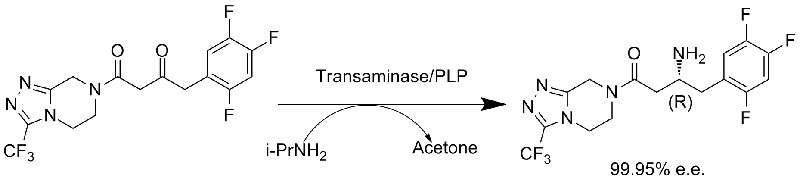
المثال 2 (ميكسيليتين، مزيج من الفصل الحركي مع التخليق غير المتماثل)(2):
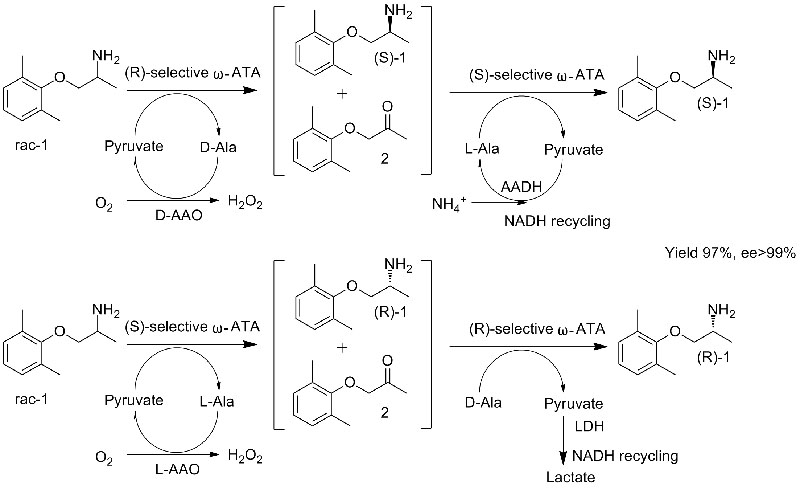
1 سافيل سي كيه، جاني جي إم، موندورف إي سي، وآخرون. ساينس، 2010، 329(16)، 305-309.
2 كوزيلوسكي د، بريسنيتز د، كلاي د، وآخرون. الرسائل العضوية، 2009،11(21):4810-4812.